如何实现纳米药物在肿瘤部位的深层渗透及有效富集,是目前肿瘤治疗中亟待办理的关键科学问题之一。研究员王浩和乔增莹发展了温度敏感型的多肽聚合物,其在血液循环中为单分子状态,由于较小的尺寸可以深层渗透到肿瘤内部;利用温敏聚合物与光热分子的结合,在近红外照射下实现了多肽聚合物在肿瘤部位的原位自组装,有效提升了纳米药物在肿瘤部位的渗透深度及富集效率(Nano Lett.2018, 18, 6577-6584)。由于肿瘤微环境呈微酸性,进一步设计合成了弱酸条件下可发生自组装的多肽聚合物,利用肿瘤微环境pH来调控其在体内的自组装行为。pH相应型的多肽聚合物能够以单链的形式渗透到实体肿瘤的深层部位,并且在肿瘤微环境弱酸的刺激下发生聚拢,规复材料较高的入胞能力,从而实现对实体肿瘤内部细胞的高效杀伤(Angew. Chem. Int. Ed.2019, 58, 4632-4637)。
生物体内的组装行为是一个非常繁芜的过程,人们面临的一项巨大寻衅是如何通过设计分子单元精准调控其体内的组装进程,从而提升药用功能。王浩、乔增莹和程冬炳利用体内重组装的调控策略,实现了纳米药物在肿瘤部位的有效富集。连接抗癌药物的纳米粒子在肿瘤部位重组装形成低级纳米纤维,其可起到“晶种”的浸染,进一步促进纳米粒子的形态转变,使纳米纤维的增长速率明显加快,从而实现抗癌药物在肿瘤部位的加速积累,为提升药物在肿瘤部位的富集供应了新策略(J. Am. Chem. Soc.2019, 141, 4406-4411)。在重组装调控的根本上,进一步发展了ROS刺激相应型的多肽聚合物,其在线粒体可以定位组装形成纳米纤维。在形态转变的过程中,治疗性肽可以通过多位点与线粒体膜发生相互浸染,极大地增强了对线粒体膜的毁坏浸染,从而有效提升肿瘤治疗效果(J. Am. Chem. Soc.2019, DOI: 10.1021/jacs.1028b07727, 封面文章)。该系列特色事情受到广泛关注,并受邀撰写综述(Acc. Chem. Res.2019, 52, 367-378)。

该系列研究得到国家自然科学基金委和中科院国际互助、交叉团队项目等的支持。
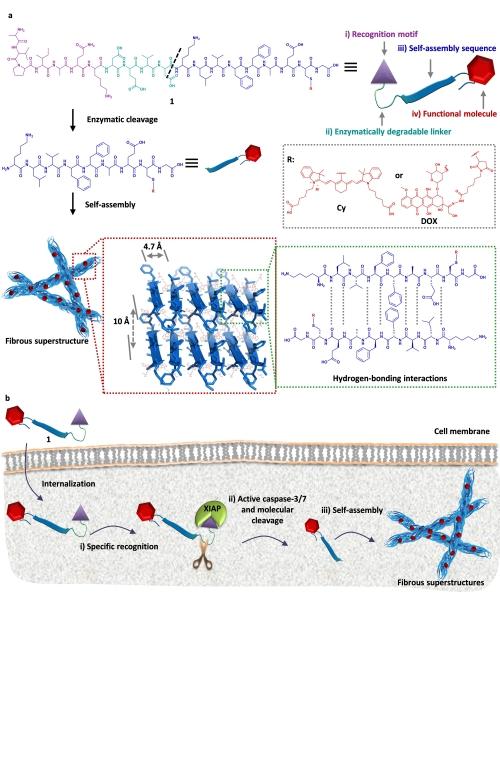
国家纳米中央在“体内自组装”多肽药物领域取得系列进展
来源:中国科学院国家纳米科学中央
温馨提示:近期,微信"大众年夜众号信息流改版。每个用户可以设置 常读订阅号,这些订阅号将以大卡片的形式展示。因此,如果不想错过“中科院之声”的文章,你一定要进行以下操作:进入“中科院之声”公众年夜众号 → 点击右上角的 ··· 菜单 → 选择「设为星标」















